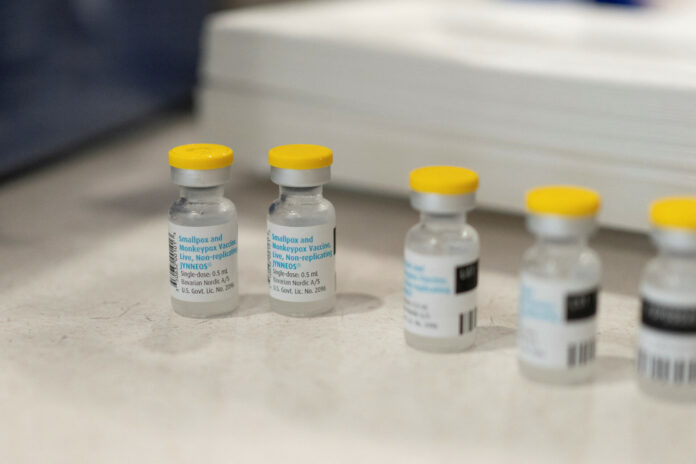
Ο Παγκόσμιος Οργανισμός Υγείας (ΠΟΥ) ανακοίνωσε το εμβόλιο MVA-BN ως το πρώτο εμβόλιο κατά της ευλογιάς πιθήκων (mpox) που θα προστεθεί στη λίστα προεπιλογών του.
Η έγκριση προεπιλογής αναμένεται να διευκολύνει την έγκαιρη και αυξημένη πρόσβαση σε αυτό το ζωτικής σημασίας προϊόν σε κοινότητες με επείγουσα ανάγκη, να μειώσει τη μετάδοση και να βοηθήσει στον περιορισμό της επιδημίας. Η αξιολόγηση του ΠΟΥ για την προεπιλογή βασίζεται σε πληροφορίες που υποβλήθηκαν από τον κατασκευαστή, τη Bavarian Nordic A/S, και την αξιολόγηση από τον Ευρωπαϊκό Οργανισμό Φαρμάκων, τον ρυθμιστικό οργανισμό καταγραφής αυτού του εμβολίου.
«Αυτή η πρώτη προεπιλογή εμβολίου κατά του mpox είναι ένα σημαντικό βήμα στον αγώνα μας κατά της νόσου, τόσο στο πλαίσιο των σημερινών κρουσμάτων στην Αφρική όσο και στο μέλλον», δήλωσε ο γενικός διευθυντής του ΠΟΥ, Δρ Tedros Adhanom Ghebreyesus και συμπλήρωσε: «Χρειαζόμαστε τώρα επείγουσα κλίμακα στις προμήθειες, τις δωρεές και την ανάπτυξη για να διασφαλίσουμε την ισότιμη πρόσβαση στα εμβόλια όπου χρειάζονται περισσότερο, μαζί με άλλα εργαλεία δημόσιας υγείας, για την πρόληψη λοιμώξεων, τη διακοπή της μετάδοσης και τη διάσωση ζωών».
Το εμβόλιο MVA-BN μπορεί να χορηγηθεί σε άτομα ηλικίας άνω των 18 ετών ως ένεση 2 δόσεων με διαφορά 4 εβδομάδων. Μετά από προηγούμενη αποθήκευση στο ψυγείο, το εμβόλιο μπορεί να διατηρηθεί στους 2–8°C για έως και 8 εβδομάδες.
Ο βοηθός γενικός διευθυντής του ΠΟΥ για την πρόσβαση σε φάρμακα και προϊόντα υγείας, Δρ Yukiko Nakatani, σημείωσε ότι η προεπιλογή του ΠΟΥ για το εμβόλιο MVA-BN θα βοηθήσει στην επιτάχυνση της συνεχιζόμενης προμήθειας των εμβολίων mpox από κυβερνήσεις και διεθνείς οργανισμούς όπως η Gavi και η Unicef για να βοηθήσουν τις κοινότητες στην πρώτη γραμμή της συνεχιζόμενης έκτακτης ανάγκης στην Αφρική και πέραν αυτής.
Η απόφαση μπορεί επίσης να βοηθήσει τις εθνικές ρυθμιστικές αρχές να επιταχύνουν τις εγκρίσεις, αυξάνοντας τελικά την πρόσβαση σε προϊόντα εμβολίου mpox με διασφάλιση ποιότητας.
Διαθέσιμα στοιχεία για τη χρήση του εμβολίου
Η Στρατηγική Συμβουλευτική Ομάδα Εμπειρογνωμόνων του ΠΟΥ (SAGE) για την ανοσοποίηση εξέτασε όλα τα διαθέσιμα στοιχεία και συνέστησε τη χρήση του εμβολίου MVA-BN στο πλαίσιο μιας εστίας mpox για άτομα με υψηλό κίνδυνο έκθεσης.
Αν και το MVA-BN δεν έχει επί του παρόντος άδεια για άτομα κάτω των 18 ετών, αυτό το εμβόλιο μπορεί να χρησιμοποιηθεί “off-label” σε βρέφη, παιδιά και εφήβους και σε έγκυες και ανοσοκατεσταλμένα άτομα. Αυτό σημαίνει ότι η χρήση εμβολίου συνιστάται σε περιβάλλον εστίασης όπου τα οφέλη του εμβολιασμού υπερτερούν των πιθανών κινδύνων.
Ο ΠΟΥ συνιστά επίσης τη χρήση μιας δόσης σε καταστάσεις έξαρσης με περιορισμό της προσφοράς. Ο ΠΟΥ τονίζει την ανάγκη συλλογής περαιτέρω δεδομένων για την ασφάλεια και την αποτελεσματικότητα του εμβολίου σε αυτές τις περιπτώσεις.
Τα διαθέσιμα δεδομένα δείχνουν ότι ένα εμβόλιο μίας δόσης MVA-BN που χορηγείται πριν από την έκθεση έχει εκτιμώμενη αποτελεσματικότητα 76% στην προστασία των ατόμων από το mpox, με το πρόγραμμα 2 δόσεων να επιτυγχάνει εκτιμώμενη αποτελεσματικότητα 82%. Ο εμβολιασμός μετά την έκθεση είναι λιγότερο αποτελεσματικός από τον εμβολιασμό πριν από την έκθεση.
Το καλό προφίλ ασφάλειας και η απόδοση του εμβολίου έχει αποδειχθεί με συνέπεια σε κλινικές μελέτες, καθώς και σε χρήση στον κοινό κατά τη διάρκεια της συνεχιζόμενης παγκόσμιας επιδημίας από το 2022. Υπό το πρίσμα της μεταβαλλόμενης επιδημιολογίας και της εμφάνισης νέων στελεχών του ιού, παραμένει σημαντικό να συλλεχθούν όσο το δυνατόν περισσότερα δεδομένα σχετικά με την ασφάλεια και την αποτελεσματικότητα των εμβολίων σε διαφορετικά πλαίσια.
Από την έναρξη της λίστας χρήσης έκτακτης ανάγκης για τα εμβόλια mpox από τον γενικό διευθυντή του ΠΟΥ στις 7 Αυγούστου 2024, ο ΠΟΥ διεξήγαγε αξιολογήσεις καταλληλόλητας προϊόντος και προγραμματισμού του εμβολίου MVA-BN.
Σύμφωνα με το Δρ Rogerio Gaspar, διευθυντή του ΠΟΥ για τη ρύθμιση και την προεπιλογή του εμβολίου, «τα ευρήματα των αξιολογήσεων είναι ιδιαίτερα σημαντικά στο πλαίσιο της κήρυξης έκτακτης ανάγκης για τη δημόσια υγεία διεθνούς ενδιαφέροντος (PHEIC) που σχετίζεται με την έξαρση του mpox στην Αφρική». Ως εκ τούτου προχωρούν οι διαδικασίες προεπιλογής και καταχώρισης χρήσης έκτακτης ανάγκης με κατασκευαστές δύο άλλων εμβολίων mpox: LC-16 και ACAM2000. «Έχουμε λάβει επίσης 6 εκδηλώσεις ενδιαφέροντος για τα διαγνωστικά προϊόντα mpox για χρήση έκτακτης ανάγκης μέχρι στιγμής’ συμπλήρωσε ο Δρ. Gaspar.
Κρούσματα σε περισσότερες από 120 χώρες
Η κλιμακούμενη επιδημία mpox στη Λαϊκή Δημοκρατία του Κονγκό και σε άλλες χώρες κηρύχθηκε «έκτακτη ανάγκη για τη δημόσια υγεία διεθνούς ενδιαφέροντος» από τον γενικό διευθυντή του ΠΟΥ στις 14 Αυγούστου 2024.
Μέχρι σήμερα πάνω από 120 χώρες έχουν επιβεβαιώσει περισσότερα από 103.000 κρούσματα mpox από την έναρξη της παγκόσμιας επιδημίας το 2022. Μόνο το 2024, υπήρχαν 25.237 ύποπτα και επιβεβαιωμένα κρούσματα και 723 θάνατοι από διαφορετικά κρούσματα σε 14 χώρες της Αφρικανικής Περιφέρειας (με βάση στοιχεία από τις 8 Σεπτεμβρίου 2024).
Σε συντονισμό με τα κράτη μέλη, ο Παγκόσμιος Οργανισμός Υγείας (ΠΟΥ) και οι εταίροι έχουν δημιουργήσει μηχανισμό πρόσβασης και κατανομής για ιατρικά αντίμετρα mpox, συμπεριλαμβανομένων εμβολίων, θεραπειών και διαγνωστικών δοκιμών. Ο Μηχανισμός Πρόσβασης και Κατανομής (AAM) θα αυξήσει την πρόσβαση σε αυτά τα εργαλεία για άτομα που διατρέχουν τον υψηλότερο κίνδυνο και θα διασφαλίσει ότι οι περιορισμένες προμήθειες χρησιμοποιούνται αποτελεσματικά και δίκαια.
Αυτό είναι μέρος της απάντησης στην έκτακτη ανάγκη για τη δημόσια υγεία διεθνούς ανησυχίας που κήρυξε ο Γενικός Διευθυντής του ΠΟΥ, Δρ Tedros Adhanom Ghebreyesus, στις 14 Αυγούστου 2024, μετά την έξαρση του mpox στη Λαϊκή Δημοκρατία του Κονγκό και στις γειτονικές χώρες. Δεκαπέντε χώρες στην Αφρική έχουν αναφέρει mpox φέτος. Οι συστάσεις που εκδόθηκαν κατόπιν συμβουλής της Επιτροπής Έκτακτης Ανάγκης για τους Διεθνείς Κανονισμούς Υγείας ζητούσαν από τα Συμβαλλόμενα Κράτη να διασφαλίσουν «ισότιμη πρόσβαση σε ασφαλή, αποτελεσματικά και διασφαλισμένα για την ποιότητα αντίμετρα για το mpox».